작가:
Mike Robinson
창조 날짜:
7 구월 2021
업데이트 날짜:
11 할 수있다 2024

콘텐츠
원자 번호는 원소의 단일 원자 핵에있는 양성자의 수에 해당합니다. 이 값은 변경되지 않습니다. 따라서 중성자 수와 같은 동위 원소의 다른 특성을 발견하는 데 사용할 수 있습니다.
단계
2 단계 중 1 : 원자 번호 찾기
주기율표의 사본을 찾으십시오. 사용할 수없는 경우 여기를 클릭하십시오. 각 요소에는 고유 한 원자 번호가 있습니다. 따라서 콘텐츠 학습에 지름길이 없습니다. 테이블의 사본을 사용하거나 암기하십시오.
- 대부분의 화학 책은 뒷면 표지에 표가 인쇄되어 있습니다.

표에서 공부하고있는 요소를 찾으십시오. 대부분의 표에는 요소의 전체 이름과 기호 (예 : 수은의 경우 Hg)가 포함되어 있습니다. 원하는 것을 찾을 수없는 경우 온라인으로 이동하여 "화학 기호"라는 용어와 요소 이름으로 검색하십시오.
원소의 원자 번호를 찾으십시오. 일반적으로 요소 집의 왼쪽 상단 또는 오른쪽 모서리에 있지만 다른 위치에도 올 수 있습니다. 또한 항상 정수 값입니다.- 숫자에 소수점이 포함 된 경우 원자 질량을 나타냅니다.
주변 요소에 따라 정보를 확인하십시오. 주기율표는 원자 번호의 순서에 따라 구성됩니다. 예를 들어 동위 원소 번호가 "33"이면 왼쪽 요소는 "32"이고 오른쪽 요소는 "34"가됩니다. 이 경우 원자 번호를보고 있기 때문입니다.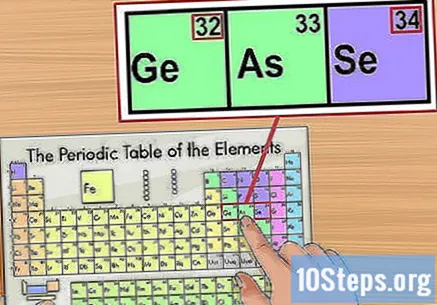
- 요소 "56"(바륨)과 "88"(라디오) 사이에 점프가 있습니다. 이 범위에 해당하는 동위 원소는 표 아래 두 행에 있습니다. 테이블이 너무 크지 않도록 이렇게 분리되어 있습니다.
원자 번호의 의미를 이해하십시오. 원자 번호는 원소의 원자에있는 양성자의 양이라는 간단한 정의를 가지고 있습니다. 이 양성자의 양은 핵의 총 전하를 결정합니다. 결과적으로 원자가 충전 할 수있는 전자의 수를 결정합니다. 전자는 거의 모든 화학적 상호 작용을 담당하기 때문에 원자 번호는 요소의 물리적 및 화학적 특성에 간접적으로 영향을 미칩니다.- 즉, 8 개의 양성자를 가진 각 원자는 산소 원자에 해당합니다. 두 개의 산소 원자는 서로 다른 수의 중성자 또는 (하나가 이온 인 경우) 또는 전자를 가질 수 있지만 항상 각각 8 개의 양성자를 가질 것입니다.
2/2 부 : 더 중요한 정보 발견
원자 무게를 결정하십시오. 일반적으로 주기율표의 요소 이름으로 제공되며 소수점 이하 두 자리 또는 세 자리가 있습니다. 원자량은 원소 원자의 평균 질량에 해당하며 자연에서 어떻게 발견되는지를 나타냅니다. "원자 질량 단위"( "u"또는 "u.m.a")로 측정됩니다.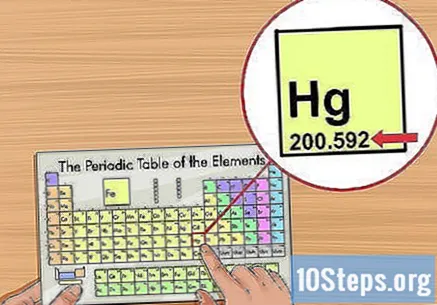
- 많은 과학자들은 무게 대신 "원자 질량"이라는 용어를 선호합니다.
원자 질량을 이해합니다. 원자 질량의 개념은 무게의 개념과 매우 유사합니다. 차이점은 무게는 특정 원자가 아니라 원소에있는 원자의 평균 질량을 나타낸다는 것입니다. 예를 들어, 철 1 그램에는 다양한 질량을 가진 여러 원자가 포함되어 있습니다. 무게는 "상대 질량"을 나타냅니다. 원소의 단일 원자를 연구하는 경우 특정 질량 만 알면됩니다.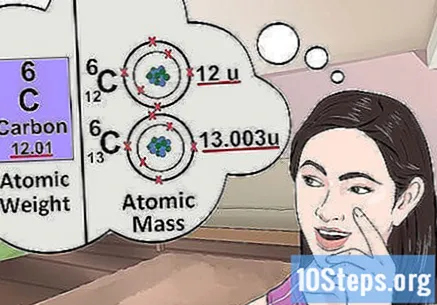
- 일반적으로 원자만을 포함하는 화학 문제는 이미 원자 질량 수를 알려줍니다. 다른 값을 볼 때 경계에 얽매이지 않도록 개념을 이해하면됩니다.
질량 수를 반올림하십시오. 질량수는 원소의 원자에서 양성자와 중성자의 총량에 해당합니다. 그것을 계산하는 것은 어렵지 않습니다. 주기율표에 인쇄 된 원자 질량을 가장 가까운 전체 값으로 반올림하십시오.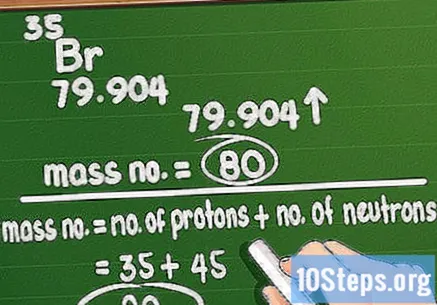
- 이것은 중성자와 양성자의 양이 1 u.m.a에 매우 가깝고 전자의 양은 0에 매우 가깝기 때문에 작동합니다. 원자 질량은 십진수 값을 결정하기 위해 정확한 계산을 포함하지만 중요한 데이터는 정수뿐입니다. 이것은 얼마나 많은 양성자와 중성자가 있는지 알려줍니다.
- 원자 질량을 사용하면 원소에서 특정 원자의 무게를 엉망으로 만들 것임을 기억하십시오. 예를 들어 브롬 샘플의 원자 질량은 79 또는 81입니다.
중성자의 수를 계산하십시오. 이제 여러분은 이미 원자 번호가 양성자의 수와 같고 질량 수가 양성자와 중성자의 수의 합과 같다는 것을 이미 알고 있습니다. 원소의 중성자의 양을 결정하려면 총 질량에서 원자 번호를 빼면됩니다. 몇 가지 예 :
- 헬륨 원자 (He)의 질량 번호는 4이고 원자 번호는 2입니다. 따라서 4-2 = 중성자 2 개.
- 은 (Ag) 샘플의 평균 질량 수는 108 (주기율표에 따름)이고 원자 번호는 47입니다. 평균적으로 샘플의 각 원자는 108-47 = 61 개의 중성자.
동위 원소 이해하기. 동위 원소는 여러 중성자를 포함하는 특정 형태의 원소입니다. 해결하고자하는 문제가 "붕소 -10"또는 "B"와 같은 것을 가져 오면 질량수가 10 인 붕소의 원소에 대해 이야기하고 있기 때문입니다. "정상"값이 아닌이 값을 사용하십시오. 붕소의.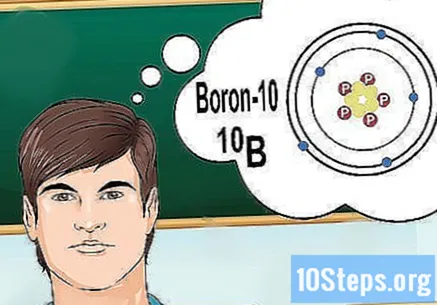
- 동위 원소의 원자 번호는 변하지 않습니다. 원소의 모든 동위 원소는 같은 수의 양성자를 가지고 있습니다.
팁
- 일부 무거운 요소의 원자량은 괄호 나 대괄호로 묶입니다. 이것은이 무게가 여러 동위 원소의 평균이 아니라 가장 안정적인 동위 원소의 정확한 질량임을 의미합니다. 마지막으로 이것은 원소의 원자 번호에 영향을 미치지 않습니다.


