콘텐츠
이 기사에서는 시행 착오 법으로 방정식 균형 맞추기 대 수법으로 방정식 균형 맞추기
화학에서, 방정식은 화학 반응 동안 일어난 일을 설정합니다. 방정식의 왼쪽에는 실험에 사용 된 시약과 실험에 사용 된 생성물을 배치합니다. 화학 반응 중 질량 (Lavoisier) 보존 원칙에 따르면 원자가 사라지지 않고 생성되지 않으며 다르게 결합합니다. 요약하면, 방정식의 왼쪽에서와 같이 오른쪽에 각 요소의 동일한 수의 원자가 있어야합니다. 그렇기 때문에 균형 방정식이 항상 균형을 이루어야합니다.
단계
방법 1 시행 착오 법에 의한 방정식의 균형
-
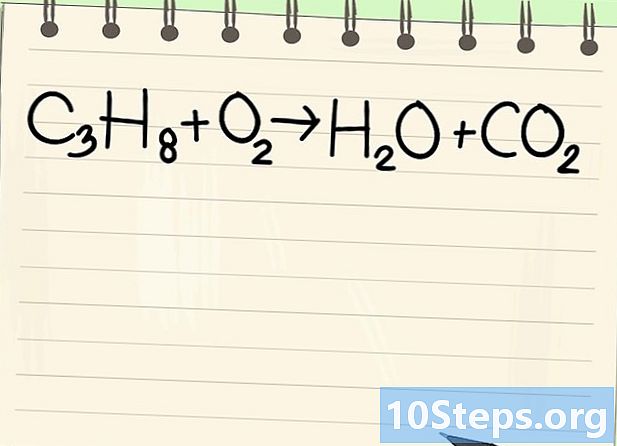
균형 방정식에 유의하십시오. 우리는 다음 방정식을 다룰 것입니다.- C3H8 + O2 -> H2O + CO2
- 이것은 프로판 연소 방정식 (C3H8) 산소에서 : 물과 이산화탄소가 얻어진다.
-
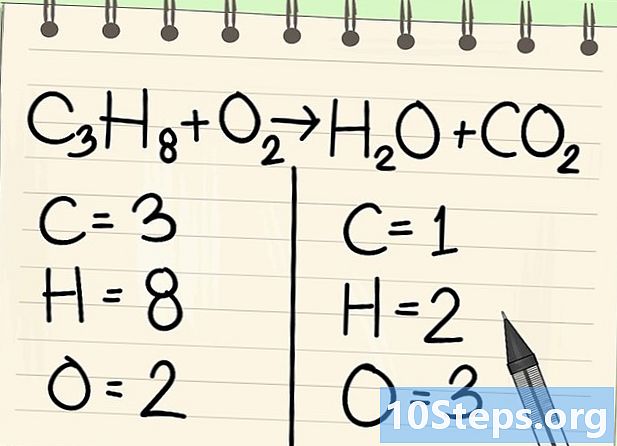
원자를 세십시오. 방정식의 한쪽에 각 요소의 데이텀 수를 입력 한 다음 다른쪽에 입력하십시오. 이를 위해 인덱스를 고려하십시오.없는 경우 인덱스는 1입니다.- 왼쪽에는 3 개의 탄소 원자, 8 개의 수소 및 2 개의 산소가 있습니다.
- 오른쪽에는 탄소 원자 1 개, 수소 2 개, 산소 3 개가 있습니다.
-
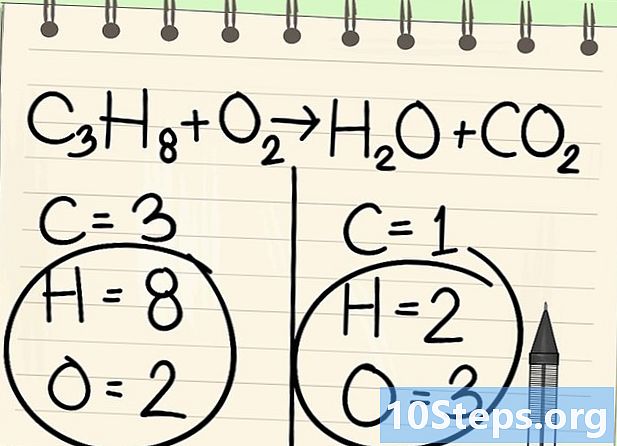
수소와 산소를 잠시 따로 두십시오. -

올바른 요소로 균형을 잡으십시오. 우리는 항상 반응 전후에 분자의 분자로 시작합니다. 여러 개가 있으면 분자 중 하나에서 1 가인 것을 선택하십시오. 여기서 우리는 탄소 원자로 시작합니다. -

탄소 원자의 균형을 잡습니다. 오른쪽에 이산화탄소 분자 (CO)에 계수를 추가하십시오2)에서 탄소 레이 톰이 단독 인 경우. 우리는 3 개의 왼쪽 원자를 얻기 위해 3을 넣을 것입니다.- C3H8 + O2 -> H2O + 3CO2
- 따라서 계수 (3CO) 덕분에 오른쪽에 3 개의 탄소 원자가 있습니다2)와 왼쪽에 3 개의 탄소 원자3H8).
- 방정식에서 원하는 모든 계수를 넣을 수 있지만 단서를 만질 수는 없습니다.
-
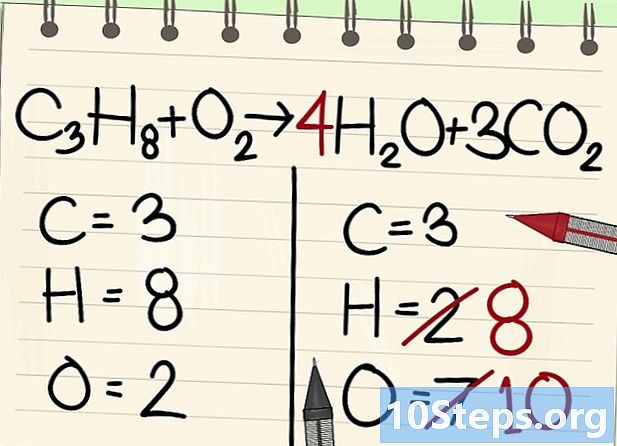
수소 원자의 균형을 잡습니다. 방정식의 왼쪽에 8이 있으므로 오른쪽이 많이 필요합니다.- C3H8 + O2 --> 4H2O + 3CO2
- 오른쪽에는 물 분자에서 수소가 2가이기 때문에 계수 4를 입력합니다. 인덱스 2는 두 개의 수소 원자가 연관되어 있음을 나타냅니다.
- 오른쪽의 수소 원자 수를 구하려면 계수 4에 지수 2 또는 8 개의 원자를 곱하십시오.
- 산소 원자에 관해서는 오른쪽에 3 개의 3CO 분자에서 나오는 6 개가 있습니다.2 (3 x 2 = 6 원자) 및 4 H의 4 분자에서 42O (4 x 1 = 4 원자), 즉 총 10 개의 산소 원자.
-
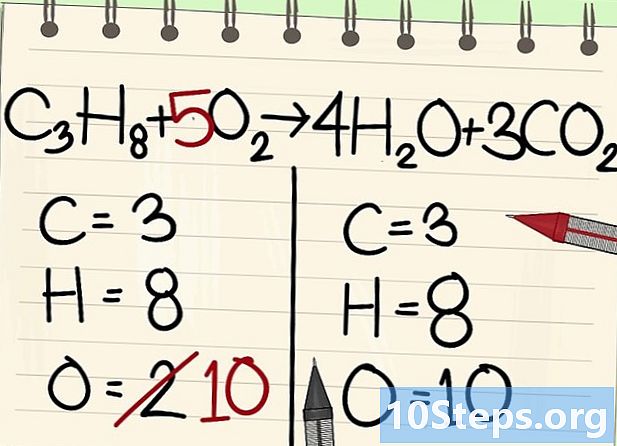
산소 원자의 균형을 잡습니다.- 탄소와 수소 균형 때문에, 산소 원자의 수는 방정식의 양변에서 동일하지 않습니다. 우리는 오른쪽에 10 개의 산소 원자가 있음을 보았습니다 (물 분자에서 4 개, 이산화탄소 분자에서 6 개). 왼쪽에는 O에서 2 개만 있습니다2).
- 산소의 균형을 맞추려면 왼쪽 산소 분자에 계수 5를 더하십시오. 왼쪽에는 10 개의 원자가 있고 오른쪽에는 다른 원자가 있습니다.
- C3H8 + 5O2 -> 4H2O + 3CO2
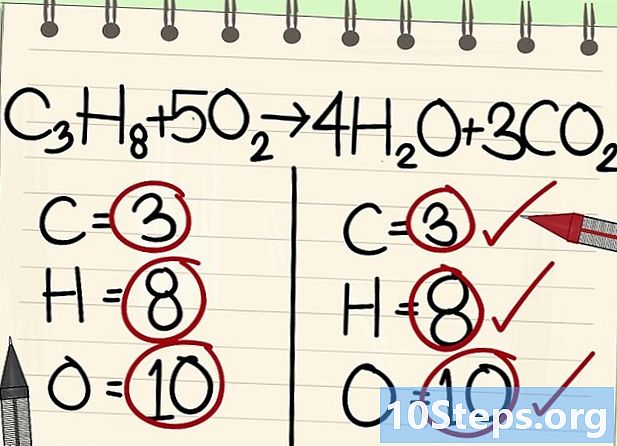
- 모든 원자 (탄소, 수소 및 산소)가 균형을 이룹니다 : 방정식의 균형이 맞습니다.
방법 2 대 수법에 의한 방정식 평형
-

균형을 잡는 방정식을 작성하십시오. 각 분자에 문자 계수를 할당하십시오. 우리는 그들을 부를 것이다 이, B, C 과 디. -
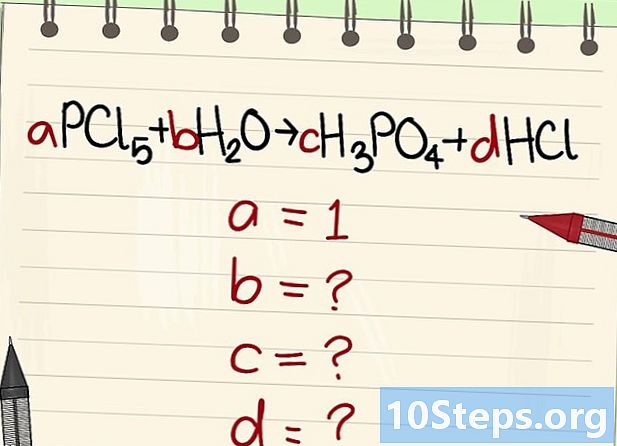
다른 리터럴 계수의 값을 찾으십시오. 우리는 그것을 요청할 것입니다 이 = 1. -

이 계수들 사이의 관계를 찾으십시오. 왼쪽 (시약)과 오른쪽 (제품)을 보면서 서로 다른 계수 사이의 관계를 설정하십시오.- 다음 방정식을 취하십시오 : aPCl5 + bH2O = cH3PO4 + dHCl. a = 1이며, 이는 c = a, d = 5a 및 2b = 3c + d를 의미합니다. 계산 완료, c = 1, d = 5 및 b = 4

- 다음 방정식을 취하십시오 : aPCl5 + bH2O = cH3PO4 + dHCl. a = 1이며, 이는 c = a, d = 5a 및 2b = 3c + d를 의미합니다. 계산 완료, c = 1, d = 5 및 b = 4