작가:
Florence Bailey
창조 날짜:
27 3 월 2021
업데이트 날짜:
1 할 수있다 2024

콘텐츠
양성자, 중성자 및 전자는 원자를 형성하는 세 가지 주요 입자입니다. 이름에서 알 수 있듯이 전자는 양전하를 띠고 후자는 전하가 없으며 (중립) 세 번째는 음전하를 띤다. 전자는 질량이 매우 적고 양성자와 중성자는 거의 동일한 질량을 가지고 있습니다. 주기율표의 정보 만 사용하여 원자에서 각각의 수를 찾을 수 있습니다.
단계
2 단계 중 1 : 양성자, 전자 및 중성자 계산
주기율표를 얻으십시오. 원자 구조로 요소를 구성하는 그림입니다. 색상별로 분류되며 각 요소에 하나, 둘 또는 세 글자의 고유 한 약어를 부여합니다. 기타 정보에는 원자 질량과 수가 포함됩니다.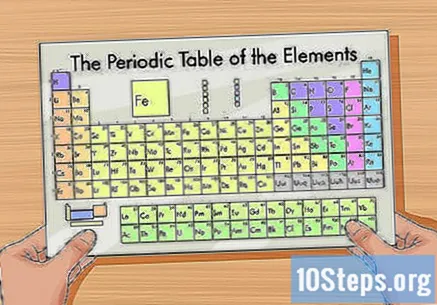
- 주기율표는 온라인이나 화학 책에서 찾을 수 있습니다.
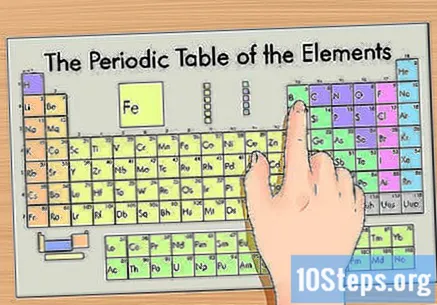
주기율표에서 원소를 찾으십시오. 원자 번호로 원소를 구성하고 금속, 비금속 및 준 금속 (반 금속)의 세 가지 주요 그룹으로 분리합니다. 다른 그룹에는 알칼리 금속, 할로겐 및 희가스가 포함됩니다.- 그룹 (열) 또는 마침표 (행)를 사용하면 표에서 요소를 더 쉽게 찾을 수 있습니다.
- 다른 속성을 모르는 경우 요소의 기호를 검색 할 수도 있습니다.
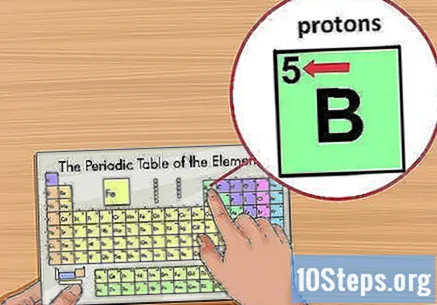
원자 번호를 찾습니다. 사각형의 왼쪽 상단 모서리에있는 요소 기호 위에 있습니다. 원자 번호는 그 원소의 단일 원자를 형성하는 양성자 수를 알려줍니다.- 예를 들어 붕소 (B)는 원자 번호가 5이므로 양성자가 5 개 있습니다.
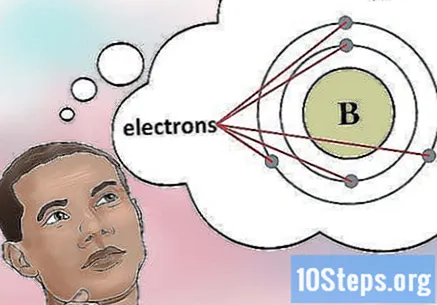
전자의 수를 결정하십시오. 양성자는 양전하를 띠는 원자핵의 입자입니다. 전자는 음으로 하전 된 입자입니다. 따라서 중성 원소는 동일한 수의 양성자와 전자를 갖습니다.- 예를 들어, 붕소 (B)는 원자 번호가 5이므로 5 개의 양성자와 5 개의 전자가 있습니다.
- 그러나 원소가 양이온 또는 음이온을 포함하는 경우 양성자와 전자는 동일하지 않습니다. 계산해야합니다. 이온 번호는 원소 뒤에 작은 위첨자로 나타납니다.
원자 질량을 찾으십시오. 중성자의 수를 찾으려면 먼저 원자 질량을 찾아야합니다. 이 값은 원소 원자의 평균 질량이며 원소 기호 아래에서 찾을 수 있습니다.
- 원자 질량을 다음 정수로 반올림합니다. 예를 들어 붕소의 원자 질량은 10.811이지만 11로 반올림 할 수 있습니다.
원자 질량에서 원자 번호를 뺍니다. 중성자의 수를 찾으려면 질량에서 원자 번호를 빼야합니다. 원자 번호는 이미 확인 된 양성자의 원자 번호와 같다는 것을 기억하십시오.
- 붕소 예의 경우 11 (원자 질량)-5 (원자 번호) = 6 중성자
2 단계 중 2 : 이온이 존재하는 전자 계산
이온 수를 확인하십시오. 요소 뒤에 작은 위첨자 값으로 나타납니다. 이온은 전자의 추가 또는 제거로 인해 양전하 또는 음전하를 띠는 원자입니다. 이온에서 양성자의 수는 동일하지만 전자의 수는 변합니다.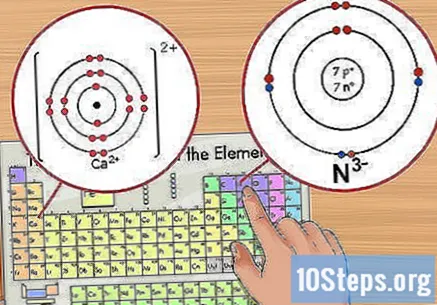
- 전자는 음전하를 띠기 때문에 제거되면 이온이 양이됩니다. 더 많은 전자가 추가되면 이온은 음이됩니다.
- 예를 들어, N에는 -3 전하가 있고 Ca에는 +2 전하가 있습니다.
- 요소 뒤에 위 첨자 번호가 없으면이 계산을 수행 할 필요가 없습니다.
원자 번호에서 전하를 뺍니다. 이온이 양전하를 띠면 원자는 전자를 잃은 것입니다. 나머지 금액을 계산하려면 원자 번호에서 추가 요금을 뺍니다. 양이온의 경우 전자보다 양성자가 더 많습니다.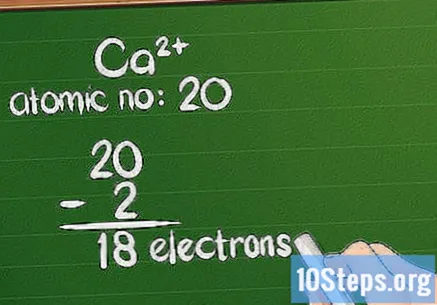
- 예를 들어, Ca는 +2 전하를 가지므로 자연 상태에서 2 개의 전자를 잃었습니다. 칼슘의 원자 번호는 20이므로 이온에는 18 개의 전자가 있습니다.
음이온의 원자 번호에 전하를 더합니다. 이온이 음전하를 띠면 원자는 전자를 얻은 것입니다. 총 개수를 계산하려면 원자 번호에 추가 요금을 더하면됩니다. 음이온의 경우 전자보다 양성자가 적습니다.
- 예를 들어 N은 -3 전하를 가지므로 중성 상태와 비교할 때 3 개의 전자를 얻었습니다. 질소의 원자 번호는 7이므로이 이온은 10 개의 전자를 가지고 있습니다.